1ĪóĖ┼─Ņ╝░Ę┤æ¬(y©®ng)▒Š┘|(zh©¼)
░č╗»īW(xu©”)─▄▐D(zhu©Żn)╗»×ķļŖ─▄Ą─čbų├Ż¼Ųõ▒Š┘|(zh©¼)╩Ū░l(f©Ī)╔·┴╦č§╗»▀ĆįŁĘ┤æ¬(y©®ng)ĪŻ
2Īóśŗ(g©░u)│╔Śl╝■
(1)ėąā╔éĆ╗Ņäėąį▓╗═¼Ą─ļŖśO(│ŻęŖ×ķĮī┘╗“╩»─½)ĪŻ
(2)īóļŖśO▓Õ╚ļļŖĮŌ┘|(zh©¼)╚▄ę║ųąĪŻ
(3)ā╔ļŖśOķgśŗ(g©░u)│╔ķ]║Ž╗ž┬Ę(ā╔ļŖśOĮėė|╗“ė├ī¦(d©Żo)ŠĆ▀BĮė)ĪŻ
(4)─▄ūį░l(f©Ī)░l(f©Ī)╔·č§╗»▀ĆįŁĘ┤æ¬(y©®ng)ĪŻ
3Īó╣żū„įŁ└Ē
╚ńłD╩ŪCu--ZnįŁļŖ│ž
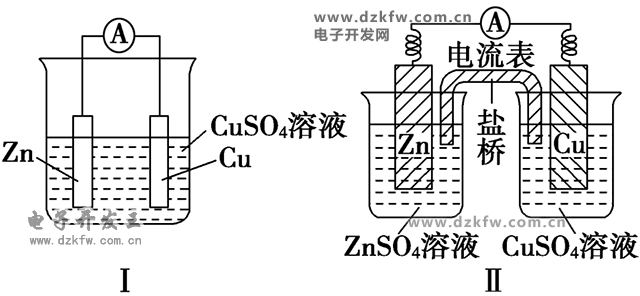
(1)Ę┤æ¬(y©®ng)įŁ└Ē
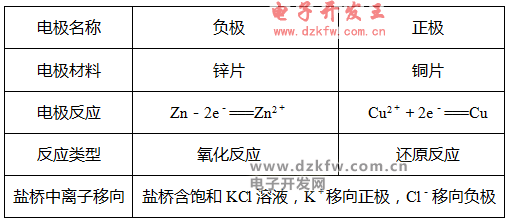
(2)įŁļŖ│žųąĄ─╚²éĆĘĮŽ“
ó┘ļŖūėĘĮŽ“Ż║Å─žō(f©┤)śO┴„│÷čžī¦(d©Żo)ŠĆ┴„╚ļš²śO;
ó┌ļŖ┴„ĘĮŽ“Ż║Å─š²śOčžī¦(d©Żo)ŠĆ┴„Ž“žō(f©┤)śO;
ó█ļxūėĄ─▀węŲĘĮŽ“Ż║ļŖĮŌ┘|(zh©¼)╚▄ę║ųąŻ¼ĻÄļxūėŽ“žō(f©┤)śO▀węŲŻ¼Ļ¢ļxūėŽ“š²śO▀węŲĪŻ
(3)ā╔ĘNčbų├Ą─▒╚▌^
łDó±ųąZnį┌CuSO4╚▄ę║ųąų▒ĮėĮėė|Cu2+Ż¼Ģ■ėąę╗▓┐ĘųZn┼cCu2+ų▒ĮėĘ┤æ¬(y©®ng)Ż¼įōčbų├ųą╝╚ėą╗»īW(xu©”)─▄║═ļŖ─▄Ą─▐D(zhu©Żn)╗»Ż¼ėųėąę╗▓┐Ęų╗»īW(xu©”)─▄▐D(zhu©Żn)╗»│╔┴╦¤ß─▄Ż¼čbų├Ą─£žČ╚Ģ■╔²Ė▀ĪŻ
łDó“ųąZn║═CuSO4╚▄ę║Ęųäeį┌ā╔éĆ│žųąŻ¼Zn┼cCu2+▓╗ų▒ĮėĮėė|Ż¼▓╗┤µį┌Zn┼cCu2+ų▒ĮėĘ┤æ¬(y©®ng)Ą─▀^│╠Ż¼╦∙ęįāH╩Ū╗»īW(xu©”)─▄▐D(zhu©Żn)╗»│╔┴╦ļŖ─▄Ż¼ļŖ┴„ĘĆ(w©¦n)Č©Ż¼Ūę│ų└m(x©┤)ĢrķgķLĪŻ
(4)¹}ś“ū„ė├
ó┘▀BĮėā╚(n©©i)ļŖ┬ĘŻ¼ą╬│╔ķ]║Ž╗ž┬Ę;
ó┌ŲĮ║ŌļŖ║╔Ż¼╩╣įŁļŖ│ž▓╗öÓ«a(ch©Żn)╔·ļŖ┴„ĪŻ
Üw╝{┐éĮY(ji©”)
1ĪóįŁļŖ│žĄ─╣żū„įŁ└Ē║åłD
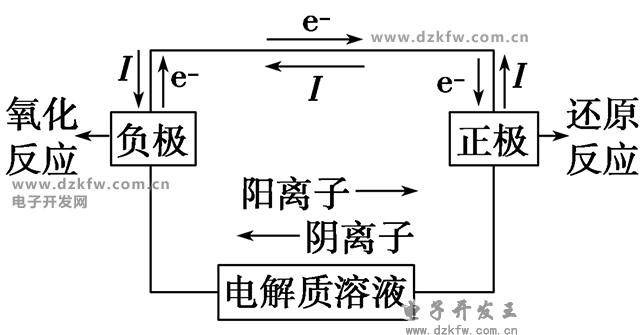
ūóęŌŻ║
ó┘ę╗░Ńžō(f©┤)śOĮī┘▌^╗ŅØŖŻ¼š²śOĮī┘╗“ĘŪĮī┘▓╗╗ŅØŖĪŻ
ó┌ę╗░Ńžō(f©┤)śO╚▄ĮŌ╗“┘|(zh©¼)┴┐£p▌pŻ¼š²śOėąÜŌ┼▌╗“┘|(zh©¼)┴┐į÷ųžĪŻ
ó█╚¶ėą¹}ś“Ż¼¹}ś“ųąĄ─ĻÄļxūėęŲŽ“žō(f©┤)śOģ^(q©▒)Ż¼Ļ¢ļxūėęŲŽ“š²śOģ^(q©▒)ĪŻ
2ĪóįŁļŖ│žĄ─┼ąöÓĘĮĘ©
(1)Ž╚Ęų╬÷ėą¤o═ŌĮėļŖį┤Ż¼ėą═ŌĮėļŖį┤Ą─×ķļŖĮŌ│žŻ¼¤o═ŌĮėļŖį┤Ą─┐╔─▄×ķįŁļŖ│žĪŻ
(2)╚╗║¾ę└ō■(j©┤)įŁļŖ│žĄ─ą╬│╔Śl╝■┼ąöÓčbų├╩Ūʱ×ķįŁļŖ│žŻ¼ĘĮĘ©╚ńŽ┬Ż║

(3)ČÓ│žŽÓ▀BŻ¼Ą½¤o═ŌĮėļŖį┤ĢrŻ¼ā╔śO╗ŅØŖąį▓Ņ«ÉūŅ┤¾Ą─ę╗│ž×ķįŁļŖ│žŻ¼Ųõ╦¹Ė„│ž┐╔┐┤ū÷ļŖĮŌ│žĪŻ
3ĪóįŁļŖ│žš²Īóžō(f©┤)śO┼ąöÓĄ─Ų▀ĘNĘĮĘ©
(1)ė╔ĮM│╔įŁļŖ│žĄ─ā╔śO▓─┴Ž┼ąöÓĪŻ
ę╗░ŃŽÓī”▌^╗ŅØŖĄ─Įī┘×ķžō(f©┤)śOŻ¼ŽÓī”▓╗╗ŅØŖĄ─Įī┘╗“─▄ī¦(d©Żo)ļŖĄ─ĘŪĮī┘×ķš²śOĪŻ
(Ą½ę▓ėąę╗ą®▓ó▓╗┼c╗ŅØŖąįę╗ų┬Ż¼╚ńMgĪóAlį┌╦ßąįĮķ┘|(zh©¼)ųąŻ¼Mgū„žō(f©┤)śOŻ¼Č°į┌ēAąįĮķ┘|(zh©¼)ųąŻ¼Alū„žō(f©┤)śO)
(2)Ė∙ō■(j©┤)ļŖ┴„ĘĮŽ“╗“ļŖūė┴„äėĘĮŽ“┼ąöÓĪŻ
į┌═ŌļŖ┬ĘŻ¼ļŖ┴„ė╔š²śO┴„Ž“žō(f©┤)śO;ļŖūėė╔žō(f©┤)śO┴„Ž“š²śOĪŻ
(3)Ė∙ō■(j©┤)įŁļŖ│ž└’ļŖĮŌ┘|(zh©¼)╚▄ę║ųąļxūėĄ─Č©Ž“ęŲäėĘĮŽ“┼ąöÓĪŻ
į┌įŁļŖ│žĄ─ļŖĮŌ┘|(zh©¼)╚▄ę║ā╚(n©©i)Ż¼Ļ¢ļxūėęŲŽ“š²śOŻ¼ĻÄļxūėęŲŽ“žō(f©┤)śOĪŻ
(4)Ė∙ō■(j©┤)įŁļŖ│žā╔śO░l(f©Ī)╔·Ą─ūā╗»üĒ┼ąöÓĪŻ
įŁļŖ│žĄ─žō(f©┤)śO░l(f©Ī)╔·č§╗»Ę┤æ¬(y©®ng)Ż¼š²śO░l(f©Ī)╔·▀ĆįŁĘ┤æ¬(y©®ng)ĪŻ
(5)XśOį÷ųž╗“£p▌pĪŻ
╣żū„║¾Ż¼XśO┘|(zh©¼)┴┐į÷╝ėŻ¼šf├„XśOėą╬’┘|(zh©¼)╬÷│÷Ż¼XśO×ķš²śO;Ę┤ų«Ż¼XśO┘|(zh©¼)┴┐£p╔┘Ż¼šf├„XśOĮī┘╚▄ĮŌŻ¼XśO×ķžō(f©┤)śOĪŻ
(6)XśOėąÜŌ¾w«a(ch©Żn)╔·ĪŻ
╣żū„║¾Ż¼XśO╔ŽėąÜŌ¾w«a(ch©Żn)╔·Ż¼ę╗░Ń╚¶░l(f©Ī)╔·┴╦╬÷│÷H2Ą─ļŖśOĘ┤æ¬(y©®ng)Ż¼šf├„XśO×ķš²śOĪŻ
(7)Ė∙ō■(j©┤)XśOĖĮĮ³pHĄ─ūā╗»üĒ┼ąöÓĪŻ
╬÷Üõ╗“╬³č§Ą─ļŖśOĘ┤æ¬(y©®ng)░l(f©Ī)╔·║¾Ż¼Š∙─▄╩╣įōļŖśOĖĮĮ³ļŖĮŌ┘|(zh©¼)╚▄ę║Ą─pHį÷┤¾Ż¼ę“Č°╣żū„║¾Ż¼XśOĖĮĮ³pHį÷┤¾┴╦Ż¼šf├„XśO×ķš²śOĪŻ


 ĘĄ╗žĒö▓┐
ĘĄ╗žĒö▓┐ ╦óą┬Ēō├µ
╦óą┬Ēō├µ Ž┬ĄĮĒōĄū
Ž┬ĄĮĒōĄū