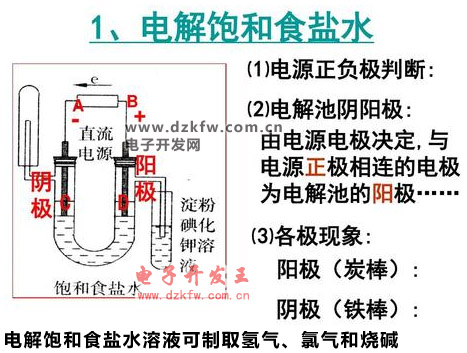
ė├▓Ż┴¦░¶š┤رØÖĄ─KIĄĒĘ█įć╝łÖz“×Ļ¢śOÜŌ¾w
(1)’¢║═╩│¹}╦«ļŖĮŌĢrŻ¼ļŖ┴„▒ĒųĖßś░l╔·Ų½▐DŻ¼ĻÄĪóĻ¢śOŠ∙ėąÜŌ¾wĘ┼│÷Ż¼Ļ¢śOÜŌ¾wėą┤╠╝żąįÜŌ╬ČŻ¼▓ó─▄╩╣رØÖĄ─KIĄĒĘ█įć╝łūā╦{Ż¼ŪęĻÄśOģ^╚▄ę║ūā╝tĪŻ
(2) Ļ¢śOŻ║2Cl-ŻŁ2e-==Cl2Ī³
ĻÄśOŻ║2H++2e-==H2Ī³(╗“2H2O+2e-==2OH-+H2Ī³)
┐éĘ┤æ¬╩ĮŻ║2NaCl+2H2O 2NaOH+H2Ī³+Cl2Ī³
(3)ĻÄśOģ^╚▄ę║ūā╝tĄ─įŁę“Ż║▀@╩Ūė╔ė┌’¢║═╩│¹}╦«ųąŻ¼╦«╦∙ļŖļx│÷Ą─H+į┌ĻÄśOĘ┼ļŖŻ¼ŲŲē─┴╦╦«Ą─ļŖļxŲĮ║Ō
(H2O H++OH-)ų┬╩╣ĻÄśOģ^ĖĮĮ³╚▄ę║ųąĄ─OH-ŽÓī”▌^ČÓŻ¼╚▄ę║│╩ēAąįŻ¼╣╩Ęė╠¬ūā╝tĪŻ
(4)└²ė├ļŖĮŌ’¢║═╩│¹}╦«╚▄ę║┐╔ųŲ╚ĪÜõÜŌĪó┬╚ÜŌ║═¤²ēAĪŻ
ļŖĮŌ’¢║═┬╚╗»Ōc╚▄ę║Ż║
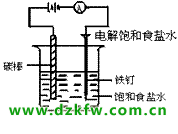
į┌ąĪ¤²▒Ł(╗“Uą═╣▄)└’čb╚ļ’¢║═╩│¹}╦«Ż¼Ą╬╚ļÄūĄ╬Ęė╠¬įćę║ĪŻė├ī¦ŠĆ░č╠╝░¶ĪóļŖ│žĪóļŖ┴„▒Ē║═ĶFßöŽÓ▀B(╚ńłD)ĪŻĮė═©ų▒┴„ļŖį┤║¾Ż¼ūóęŌė^▓ņļŖ┴„▒ĒĄ─ųĖßś╩ŪʱŲ½▐DŻ¼ęį╝░ąĪ¤²▒Łā╚░l╔·Ą─¼FŽ¾Ż¼▓óė├رØÖĄ─ĄŌ╗»ŌøĄĒĘ█įć╝łÖz“×Ļ¢śOĘ┼│÷Ą─ÜŌ¾wĪŻ
ūóŻ║┤ųĶFßöę¬┼cų▒┴„ļŖį┤Ą─ĻÄśOŽÓ▀BŻ¼╠╝░¶┼cĻ¢śOŽÓ▀BĪŻ


 ĘĄ╗žĒö▓┐
ĘĄ╗žĒö▓┐ ╦óą┬Ēō├µ
╦óą┬Ēō├µ Ž┬ĄĮĒōĄū
Ž┬ĄĮĒōĄū